ゲノムの時代へ
膨大な情報を、
わたしたちは自在にあやつって、
新しい時代を拓くことができるのか、
やがてくる明日への羅針盤に
稀少疾患の原因探索に使われる日本人全ゲノムのバリアント頻度パネル
図を拡大
 ヒトはおよそ30億塩基対の配列をもっています。そのうち、たとえば一個人を見ると、常染色体で平均約420万箇所の塩基が、国際的な参照用配列に比べて異なります。その異なる部分をバリアントと呼び、集団が異なると、バリアントの組み合わせも異なることが分かっています。このバリアントの頻度について、世界的にいくつかの民族集団で調査が行われており、民族集団毎(例えばアフリカ系、東アジア系など)にまとめたデータベースが存在します。gnomADデータベースはその代表的なものの一つで、全ゲノムでは約1.5万人、遺伝子領域に絞ったもの(エクソーム)では約12.6万人を対象とした大規模データベースとなっています。
ヒトはおよそ30億塩基対の配列をもっています。そのうち、たとえば一個人を見ると、常染色体で平均約420万箇所の塩基が、国際的な参照用配列に比べて異なります。その異なる部分をバリアントと呼び、集団が異なると、バリアントの組み合わせも異なることが分かっています。このバリアントの頻度について、世界的にいくつかの民族集団で調査が行われており、民族集団毎(例えばアフリカ系、東アジア系など)にまとめたデータベースが存在します。gnomADデータベースはその代表的なものの一つで、全ゲノムでは約1.5万人、遺伝子領域に絞ったもの(エクソーム)では約12.6万人を対象とした大規模データベースとなっています。
一方、原因のよくわかっていない、稀な病気の要因を探るための遺伝子解析をする機会が現在増えつつあります。例えば、とある症状の方の遺伝子解析を行った結果、遺伝子領域で数万箇所のバリアントが検出されたとします。さて、この中から病気の原因になるバリアントはあるでしょうか、というのが解析目的のひとつです。原因バリアントがわかると、そのバリアントが属する遺伝子の機能や、バリアントに起因するタンパク質の機能変化などから病気の遺伝的背景が明らかになり、効果的な治療法を選択する足がかりになるからです。実際に、診断の難しい患者さんに対して、家族性も考慮して遺伝的要因を探る試みが日本で行われています (未診断疾患イニシアチブ IRUD)。
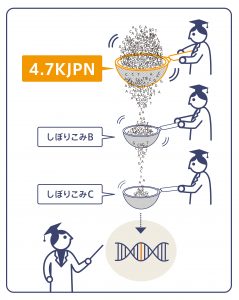
では、この病気の要因を探る遺伝子解析で、実際には数万の候補のほとんど(あるいはすべて)が、対象の病気と直接関係がないバリアントであろうことが想定される中、どのように原因バリアントを探すのでしょうか。最終候補へと絞り込んでいくその際に利用されるのが、バリアントを集めた大規模データベースなのです。特に稀な病気の場合は、集団である程度の頻度でみられるバリアントは、特定の病気と関連づけられないと推定されます。このことから、数万の病気の原因バリアント候補のうち、集団である程度(例えば1%以上)の頻度で見られるバリアントをふるいおとせるのです。
ただ人類の歴史的な背景から、民族集団によってバリアント頻度は異なり、特定の民族集団でのみ多くみられるバリアントは多々あるのです。したがって、解析対象の方が日本人であれば、日本人集団の頻度データを用いることで、より絞り込みの精度が上がることが考えられます。しかしながら、世界最大規模のデータベースgnomADにおいて、日本人由来の数は約80人程度と少ない状況です。東北大学東北メディカル・メガバンク機構(ToMMo)では日本人を対象としたバリアントデータベースを公開しており、2019年には対象を約4,700人に増やした全ゲノムのバリアント頻度パネル(4.7KJPN)を公開しました。ToMMoのバリアント頻度パネルは、これまで国内の各種の疾患研究において原因バリアントの絞り込みに活用されてきています。このように、病気の原因バリアントの同定に、住民コホートから得られたバリアント頻度パネルは重要な役割を果たすことができるのです。
【関連リンク】
最新記事一覧
-
- きこえと遺伝子医療の現在
- 2025.12.26|宇佐美真一
-
- 人体を取りまく常在菌〜機能を知って共存しよう〜
- 2020.12.16|後藤まき
-
- なぜウイルスははやく変化するのか?
- 2020.09.08|山口由美
-
- 棒状で増やすか環状で増やすか―新たなシークエンサー開発―
- 2020.07.16|川嶋順子
-
- 新型コロナウイルスに対する抗体
- 2020.05.18|峯岸直子

